|
Estudo da Eletrosfera
(Modelo atômico orbital)
·
Princípio da dualidade de De Broglie:
o elétron assume o comportamento, às vezes de onda, às vezes de
partícula. O elétron é considerado uma "partícula-onda."
·
Princípio de incerteza de Heinsenberg:
não é possível determinar, com certeza, a posição e a velocidade
de um elétron no mesmo instante.
·
Equações de Schörindger: orbital é a região
no espaço atômico onde há maior probabilidade de se encontrar um
elétron.
Orbital do tipo "s" esférica
Orbital do tipo "p" em halteres
·
Princípio da Exclusão de Pauli:
num mesmo orbital pode-se ter no máximo 2 elétrons, de rotações
("spins") contrários.
·
Diagrama de Linus-Pauling: usado
para distribuir os elétrons pelos subníveis energéticos em ordem
crescente de energia.
·
Regra de Hund: usada para
distribuir os elétrons pelos orbitais.

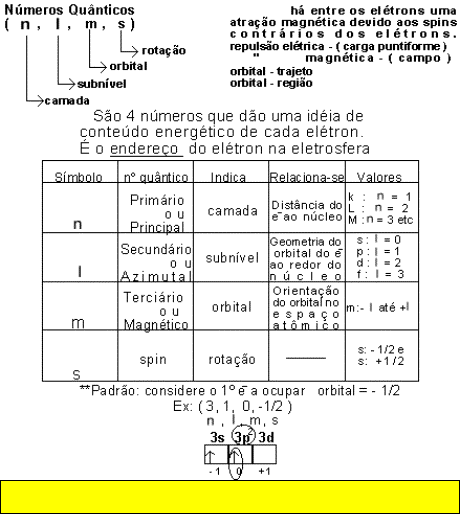
- Princípio
da Exclusão de Pauli "II":
num mesmo átomo é impossível ter dois elétrons com mesmo conjunto
de números quânticos.
|



